|
Nach den Forschungen von Francois Jacob und Jacques Monod
und dem von den beiden Forschern aufgestellten Schema vollzieht sich die
Regulation der Proteinsynthese nach einem bestimmten Mechanismus. Das Jacob-Monod-Modell war der erste entdeckte und entschlüsselte Genregulationsmecahnismus. Inzwischen sind zahlreiche andere Modelle dazu gekommen.
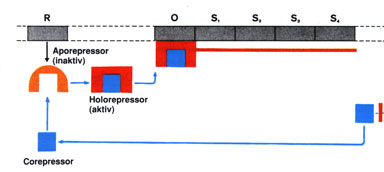
Abb.: Das Regulatorgen R produziert ein Molekül, einen inaktiven
Aporepressor. Wenn sich dieser Aporepressor mit einem Corepressor
(einem Substrat) verbindet, so entsteht ein aktiver Holorepressor,
der den Operator verschließt. Die Ablesung der Strukturgene S1,
S2, ... usw. wird dadurch verhindert. (Der rote Strich symbolisiert
die Ableseblockade).
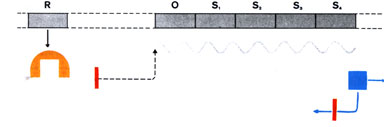
Abb.: Wird das Endprodukt (das oben erwähnte Substrat) sofort weiterverarbeitet,
kann sich kein Holorepressor bilden. Das Ablesen der Informationen
der Strukturgene S1, S2, ... usw. und somit die damit verbundene Enzymproduktion
gehen weiter.
Es muss neben den Genen für die Synthese der Enzyme noch besondere
Gene geben, die für die Regulierung der Aktivität dieser Enzymgene
verantwortlich sind. Durch Genkartierung beim Bakterium Escherichia coli
wurde festgestellt, dass die Gene, die die Struktur eines spezifischen
Proteins bestimmen, stets unmittelbar nebeneinander liegen; sie heißen
daher Strukturgene, werden auch stets gemeinsam "abgelesen",
und bei der Transkription entsteht eine einzige m-RNA.
Die Ablesung der Strukturgene wird von dem Protein eines weiteren
Gens, dem Regulatorgen, gesteuert. Dieses Protein hemmt die Ablesung
der Strukturgene und wird als Repressor bezeichnet.
Der Repressor wirkt spezifisch auf die ihm jeweils zugeordnete Strukturgene,
tritt also mit ihnen in Wechselwirkung. Dies wird durch ein benachbartes
DNA-Stück, das als Operator bezeichnet wird, erreicht.
Neben diesem liegt ein weiterer kurzer DNA-Abschnitt, der als Anlagerungsstelle
für die RNA-Polymerase dient. Operator und Strukturgene zusammen
bilden ein Operon. Wenn sich ein Repressormolekül an den Operator
anlagert, kann die RNA-Polymerase nicht gebunden werden. Damit wird die
Synthese der m-RNA an den Strukturgenen unterbunden. (Zur Erinnerung:
Die m-RNA transportiert den genetischen Code aus dem Zellkern ins Plasma,
wo die Proteine synthetisiert werden).
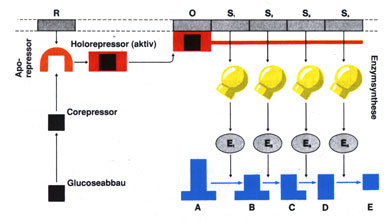
Abb.: Wenn der Corepressor aus dem Glucoseabbau kommt, dann
verbindet er sich mit dem (noch inaktiven) Aporepressor zum (jetzt
aktiven) Holorepressor und blockiert das Operon (Operon
= Operatorgen + Strukturgene). Die Enzymsynthese wird eingestellt. (Die
kugeligen gelben Gebilde symbolisieren die Ribosomen, an denen die Enzyme
entstehen).
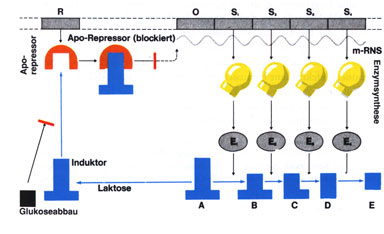
Abb.: Wenn aus dem Glucoseabbau kein oder zu wenig Corepressor kommt,
dann verbindet sich die Ausgangssubstanz (hier der Zucker Laktose) mit
dem Aporepressor zu einer unwirksamen Verbindung. Der Aporepressor bleibt
unwirksam. Die Strukturgene S1, S2, ... usw. werden gelesen und umgesetzt.
Die Synthese der Enzyme E1, E2, ... usw. (hier sind es Laktose abbauende
Enzyme) beginnt.
Wird die Raumstruktur des Repressors verändert, sodass er
mit dem Operator nicht mehr in Wechselwirkung treten kann, wird die
Blockierung des Operators aufgehoben, m-RNA kann gebildet werden,
und die Synthese des von dem gesamten Operon aufgebauten Endproduktes
läuft an.
Vor allem bei der Synthese von Enzymen für abbauende Stoffwechselreaktionen
erfolgt die Steuerung der Genaktivität durch Substratinduktion;
d. h. die Auslösung der Enzymsynthese wird durch das Substrat bewirkt,
das als Induktor fungiert.
Eine andere Möglichkeit der Regulation ist die Hemmung vom Endprodukt
her: Wird das Endprodukt in der Zelle nicht weiterverwertet und
reichert sich daher an, wirkt es als Corepressor. Dadurch
wird der Repressor in seiner Form verändert, lagert sich an den Operator
und verhindert so die weitere Transkription der Strukturgene.
|

